近日,我实验室王兆慧研究员团队在环境期刊ACS ES&T Water在线发表了题为“Undiscovered spin trapping artifacts in persulfate oxidation processes: implications for identification of hydroxyl or sulfate radicals in water”(DOI: https://doi.org/10.1021/acsestwater.2c00554)的研究论文。该研究工作首次报道了过硫酸盐(PDS)与自由基捕获剂5,5-二甲基-1-吡咯啉-N-氧化物(DMPO)或N-叔丁基-α-苯基硝酮(PBN)可能产生EPR伪信号的反应路径。这一发现表明,在探究催化氧化过程反应机理时选择合适的自旋捕获剂和严格控制对比实验的必要性。
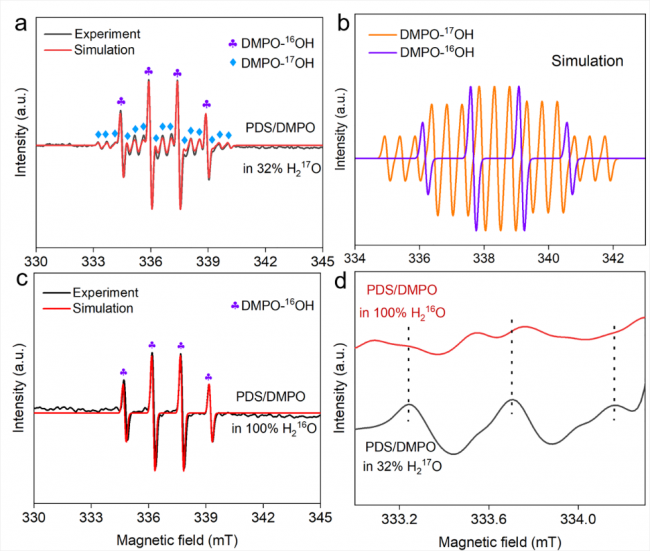
图1. 有无17O水的PDS/DMPO体系的EPR谱图及低场谱区。
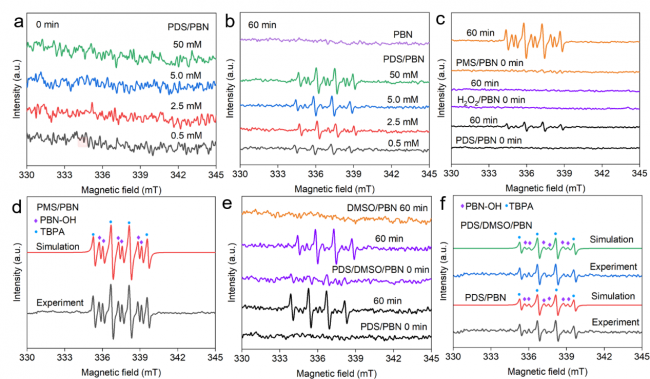
图2. 不同PDS浓度下PDS/PBN体系的初始EPR信号(a)和60 min时的信号(b)。(c)在相同反应条件下PDS/PBN、H2O2/PBN、PMS/PBN体系产生的信号以及(d)PMS/PBN体系的模拟信号。(e)PDS/PBN体系的淬灭实验以及(f)相应信号的模拟。
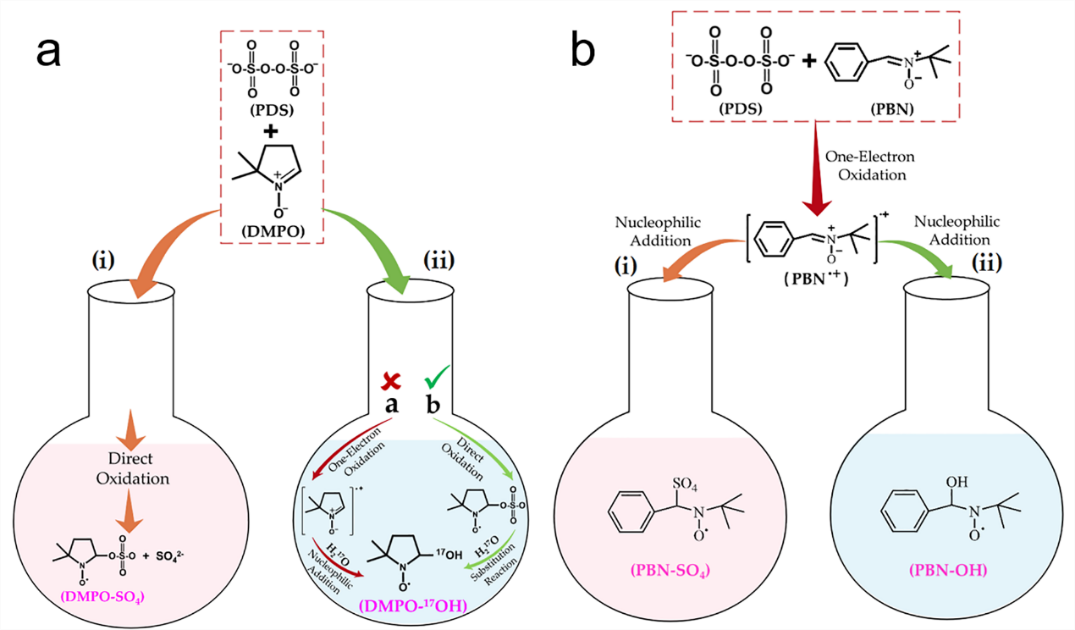
图3. 以乙腈、丙酮(i)或H2O(ii)为溶剂的PDS/DMPO和PDS/PBN体系中主要加合物的生成路径。
图3展示了DMPO-OH、DMPO-SO4、PBN-OH和PBN-SO4加合物的详细产生路径。在以水为溶剂的PDS/DMPO体系中,DMPO-OH的生成可能通过两种途径(图3a,(ii)):a,反向自旋捕获机制;b,直接氧化和H2O的取代反应。在路径a中,PDS首先通过单电子氧化DMPO,然后与H2O发生亲核加成反应,生成DMPO-OH。H2O是一种具有反应活性的亲核试剂,可与DMPO•+亲电试剂反应生成DMPO-OH。DMPO•+可以与MeOH反应生成MeOH衍生的加合物(DMPO-OCH3)。然而,在PDS/DMPO体系中加入MeOH后,没有出现DMPO-OCH3加合物且DMPO-OH信号未见衰减,说明路径a(图3a中红色×标记)不可行。因此,我们提出了更合理的路径b(图3a中绿色√),DMPO-SO4在水的作用下转化为DMPO-OH,17O同位素标记实验和密度泛函理论计算(DFT)证明了这一点。在PDS/DMPO体系中,整个反应过程并不涉及“真正的”自由基。根据溶剂实验,我们得出DMPO-OH或DMPO-SO4加合物的主导地位取决于水的量。例如,在乙腈/H2O混合溶剂中(如25%/75%,v/v),可以同时检测到DMPO-OH和DMPO-SO4,因此路径(i)和(ii)同时进行(如图3a)。一旦H2O的占比超过乙腈,则(ii)占主导地位,因此无法观察到可识别的DMPO-SO4信号。同样,在丙酮溶剂中,DMPO-SO4也是主要信号。在PDS/MeOH/PBN体系中可以检测到PBN-OCH3信号,说明PDS可以通过单电子氧化作用将PBN氧化生成PBN•+,进而在乙腈或丙酮溶剂中生成PBN-SO4,或在H2O溶剂中通过亲核加成反应生成PBN-OH(图3b)。
上述工作采用淬灭实验与EPR相结合的方法研究了自旋加合物的形成途径,通过17O同位素标记实验验证了DMPO-OH中的羟基氧完全来自于水。反应时间、PDS浓度、以及反应溶剂均对反应体系产生的信号有重要影响。由于在过硫酸盐氧化体系中,几乎所有的反应机制都依赖于自旋捕获技术鉴定自由基,因此,我们提醒研究同行们在基于PDS的催化体系鉴定自由基时要格外谨慎。
华东师范大学博士生王玲利为第一作者,王兆慧研究员为唯一通讯作者,澳大利亚昆士兰理工大学朱怀勇教授和南非约翰内斯堡大学Mika Sillanpää教授为共同作者。该研究工作得到了上海市科委“科技创新行动计划”、“一带一路”青年科学家交流国际合作项目和国家重点研发计划项目的资助。
论文链接:https://pubs.acs.org/doi/pdf/10.1021/acsestwater.2c00554